[Vorgeschlagene Verwendung]
Der Troponin I (cTnI) Rapid Test (Vollblut/Serum/Plasma) ist ein schneller visueller Immuntest zur qualitativen und vermutlichen Erkennung von Herztroponin I im menschlichen Vollblut.Serum- oder PlasmaprobenEs ist zur Anwendung als Hilfsmittel bei der Diagnose von Myokardinfarkt (MI) bestimmt.
[Einleitung]
Troponin I (cTnI) ist ein Protein im Herzmuskel mit einem Molekulargewicht von 22,5 kDa. Troponin I ist Teil eines drei-Untereinheit-Komplexes, bestehend aus Troponin T und Troponin C.Zusammen mit Tropomyosin, bildet dieser Strukturkomplex die Hauptteilkomponente, die die kalziumsempfindliche ATPase-Aktivität von Aktomyosin im gestreiften Skelett- und Herzmuskel reguliert.Troponin I wird 4-6 Stunden nach Schmerzbeginn ins Blut freigesetzt.Das Freisetzungsmuster von cTnI ähnelt dem von CK-MB, aber während der CK-MB-Spiegel nach 72 Stunden wieder normal wird, bleibt Troponin I 6-10 Tage lang erhöht.so dass ein längeres Zeitfenster zur Erkennung von Herzverletzungen bestehtDie hohe Spezifität von cTnI-Messungen zur Identifizierung von Myokardschäden wurde unter Umständen wie der perioperativen Periode, nach Marathonläufen,und stumpfes Brusttrauma. cTnI-Release wurde auch bei anderen Herzerkrankungen als einem akuten Myokardinfarkt (AMI) wie instabiler Angina pectoris, kongestiver Herzinsuffizienz,und ischämische Schäden aufgrund von KoronararterienbypassoperationenAufgrund seiner hohen Spezifität und Empfindlichkeit im Myokardgewebe ist Troponin I in jüngster Zeit zum bevorzugten Biomarker für Myokardinfarkt geworden.
[Hauptinhalte]
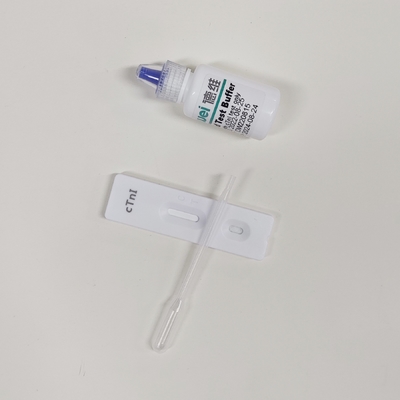
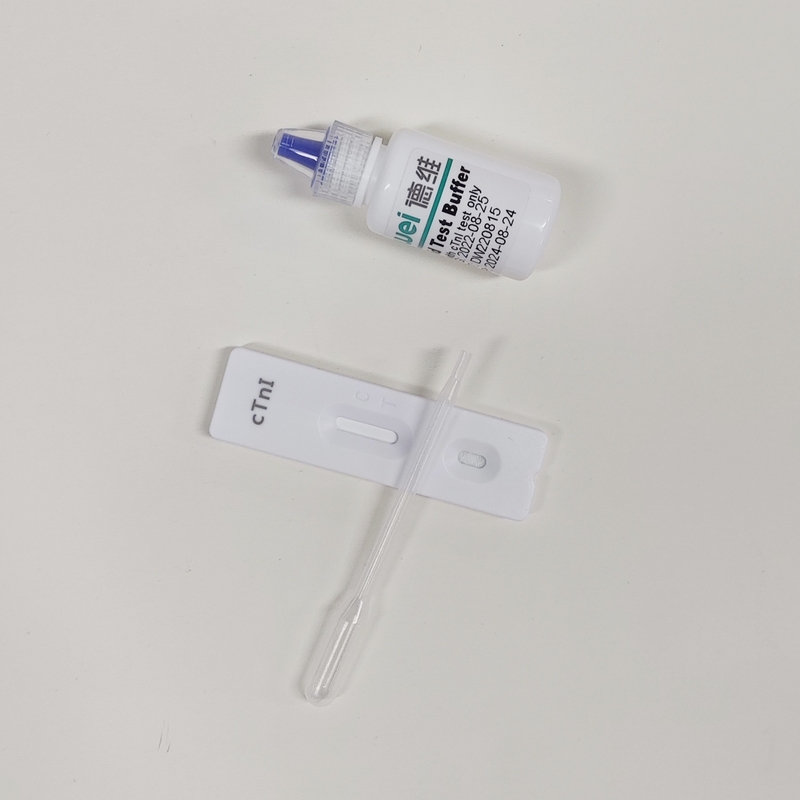
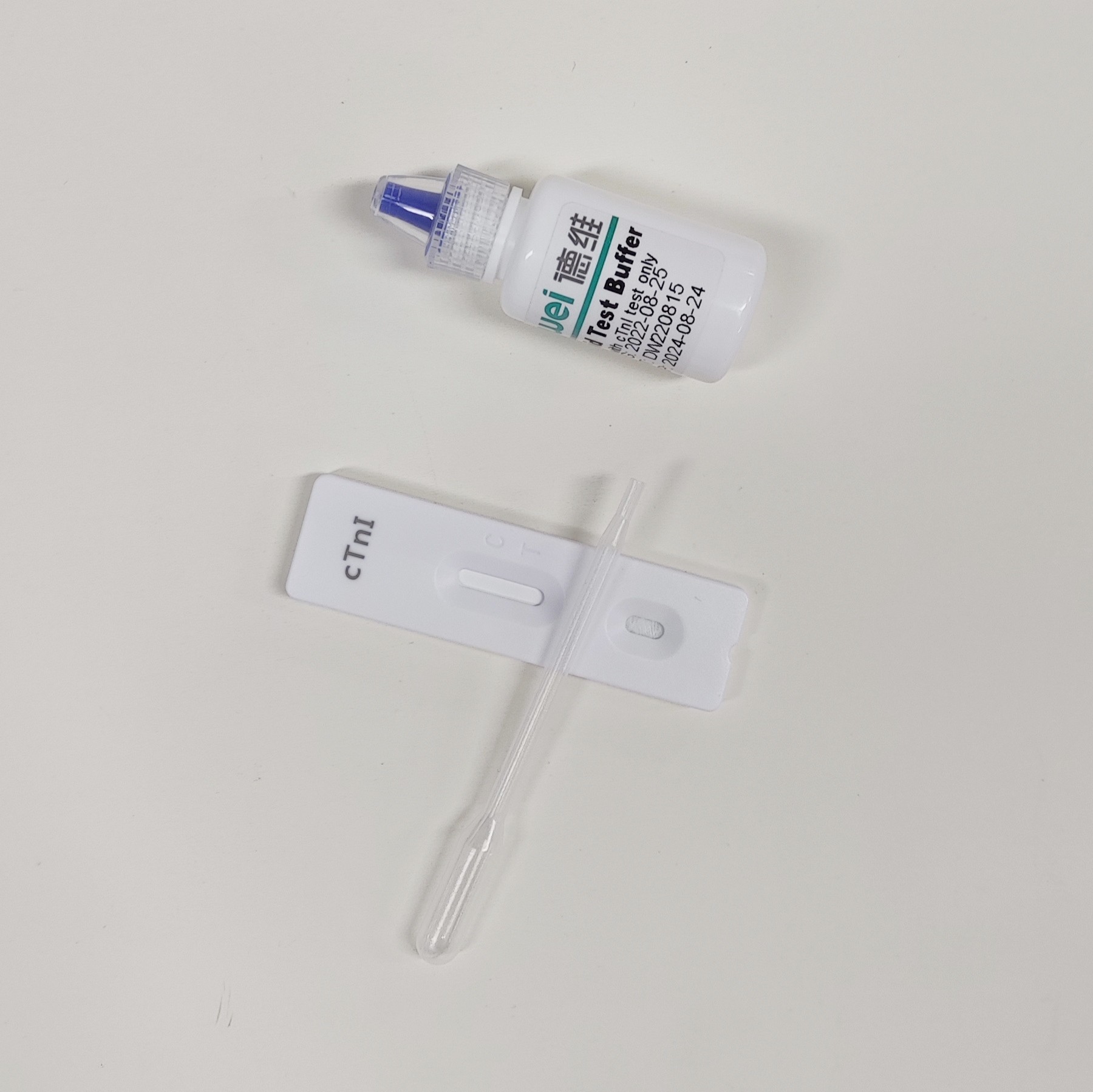
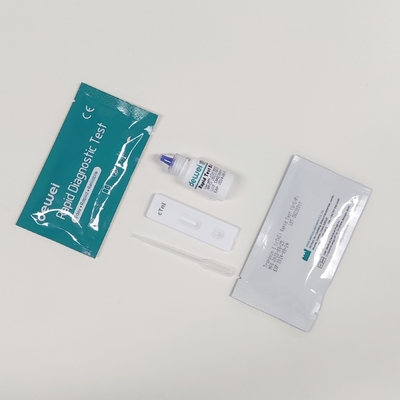
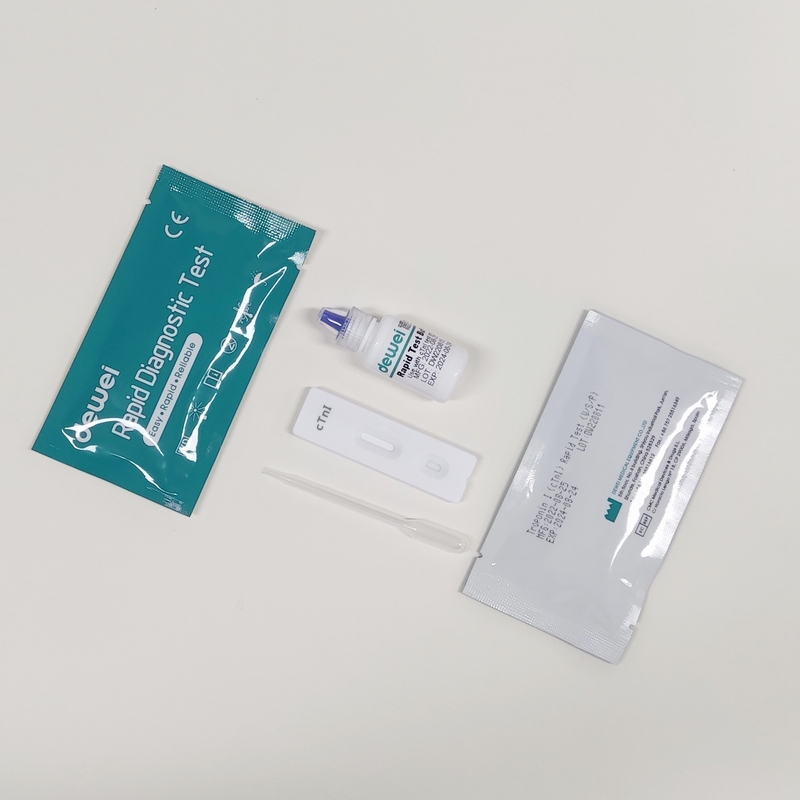
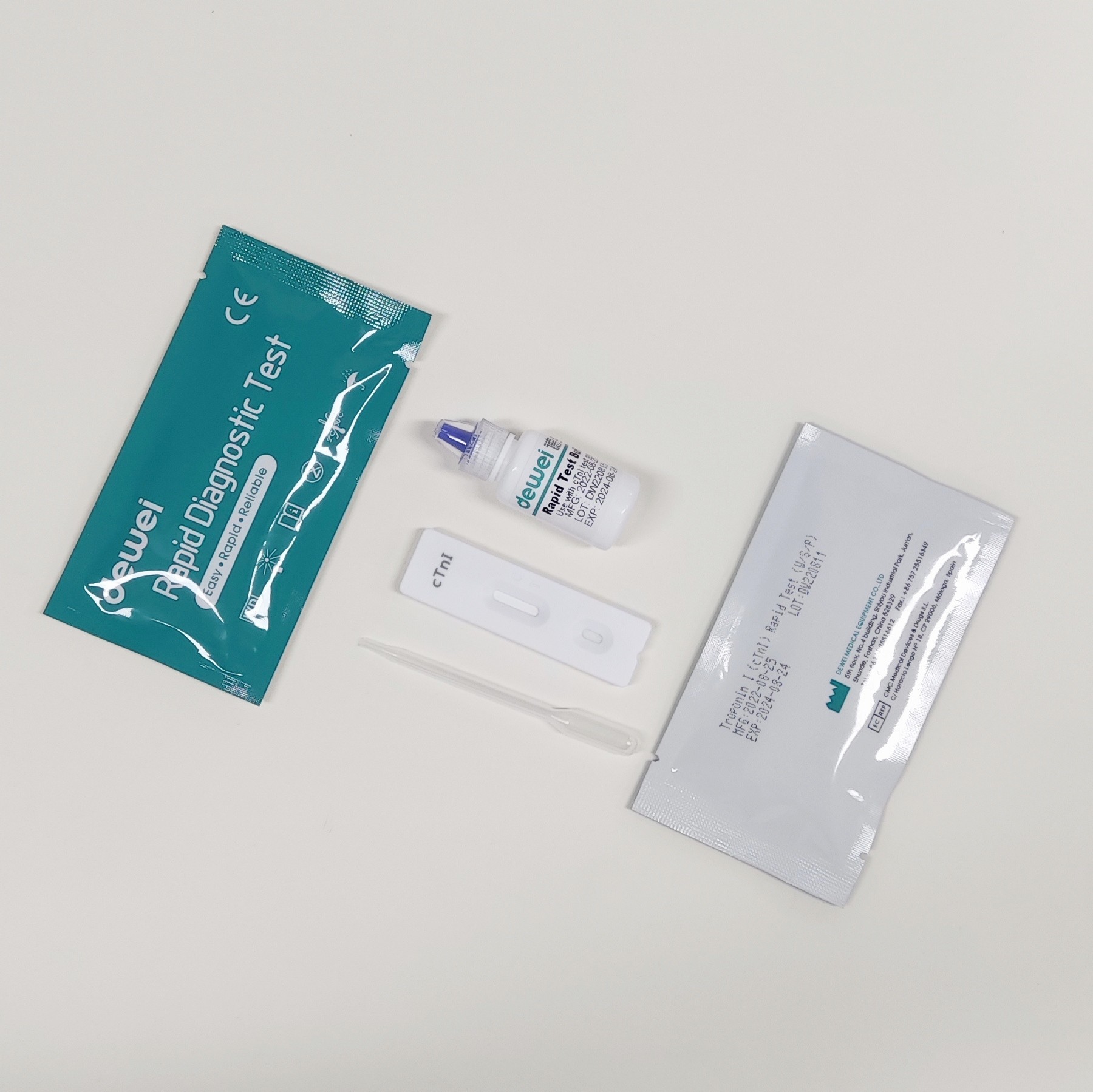
• Schnelltestkassette mit Trocknungsmittel
• Einwegpipetten
• Puffer
• Packungsbeilage
[VORSORGEN]
• Nur für die professionelle In-vitro-Diagnostik.
• Verwenden Sie den Test nicht nach dem auf der Verpackung angegebenen Verfallsdatum.
• Dieses Kit enthält Produkte tierischen Ursprungs, wobei eine zertifizierte Kenntnis der Herkunft und/oder des hygienischen Zustands der Tiere nicht die vollständige Abwesenheit von übertragbaren Krankheitserregern garantiert.Es ist daher, empfohlen, diese Produkte als potenziell infektiös zu behandeln und unter Beachtung der üblichen Sicherheitsvorkehrungen (z. B. nicht einnehmen oder einatmen) zu behandeln.
• Vermeiden Sie eine Kreuzkontamination der Proben, indem Sie für jede gewonnenen Probe einen neuen Probenentnahmebehälter verwenden.
• Lesen Sie das gesamte Verfahren vor dem Test sorgfältig durch.
• Essen, trinken oder rauchen Sie nicht in der Umgebung, in der die Proben und Kits behandelt werden.Beobachten Sie während des gesamten Verfahrens die vorgegebenen Vorsichtsmaßnahmen gegen mikrobiologische Gefahren und befolgen Sie die Standardverfahren für die ordnungsgemäße Beseitigung der Proben.- Verwenden Sie bei der Untersuchung von Proben Schutzkleidung wie Labormantel, Einweghandschuhe und Augenschutz.
• Feuchtigkeit und Temperatur können sich negativ auf die Ergebnisse auswirken.
• Verwendete Prüfmaterialien sollten gemäß den örtlichen Vorschriften entsorgt werden.
[Speicherung und Stabilität]
• In der verschlossenen Packung für 24 Monate bei 2 ~ 30 °C aufbewahren.
• Nicht direktem Sonnenlicht, Feuchtigkeit und Hitze ausgesetzt
• FREESEN Sie nicht ein.
[PROBELSAMPLEN]
•Der Troponin I (cTnI) Rapid Test ist nur für die Anwendung mit menschlichem Vollblut, Serum oder Plasma bestimmt.
•Nur durchsichtige, nicht hämolysierte Proben sind für diesen Test zu empfehlen.
•Testen Sie unmittelbar nach der Probenabnahme. Lassen Sie die Proben nicht länger bei Raumtemperatur liegen. Serum- und Plasmaproben können bis zu 3 Tage bei 2-8°C aufbewahrt werden.Für die langfristige LagerungWenn der Test innerhalb von 2 Tagen nach der Sammlung durchgeführt werden soll, sollte das durch Venenpunktion entnommene Vollblut bei 2-8°C aufbewahrt werden.Vollblut, das durch Fingerstick gesammelt wurde, sollte sofort untersucht werden..
•Behälter mit Antikoagulanzien wie EDTA, Zitrat oder Heparin sollten zur Lagerung von Vollblut verwendet werden.
•Vor der Prüfung müssen die Proben auf Raumtemperatur gebracht werden. Gefrorene Proben müssen vor der Prüfung vollständig aufgetaut und gut gemischt werden. Wiederholtes Einfrieren und Auftauen von Proben ist zu vermeiden.
•Wenn Proben versandt werden sollen, müssen sie in Übereinstimmung mit allen geltenden Vorschriften für den Transport ätiologischer Erreger verpackt werden.Wärmebehandelte und kontaminierte Proben können zu falschen Ergebnissen führen.
•Es besteht eine geringe Möglichkeit, dass einige Vollblutproben mit sehr hoher Viskosität oder die länger als 2 Tage aufbewahrt wurden, nicht ordnungsgemäß am Testgerät laufen.Der Test mit einer Serum- oder Plasmaprobe des gleichen Patienten mit einem neuen Prüfgerät wiederholen.
[Anwendungsrichtung]
Vor der Anwendung müssen Prüfungen, Proben, Puffer und/oder Kontrollen auf Raumtemperatur (15-30°C) gebracht werden.
1. Entfernen Sie den Test aus dem versiegelten Beutel und legen Sie ihn auf eine saubere, ebene Oberfläche.Der Test sollte innerhalb einer Stunde durchgeführt werden..
2Übertragen Sie 1 Tropfen Vollblut-, Serum- oder Plasmaprobe mit der mitgelieferten Einwegpipette in den Probenbrunnen (S) des Geräts, fügen Sie dann 1 Tropfen Puffer hinzu und starten Sie den Timer.Vermeiden Sie das Einfangen von Luftblasen im Probenbrunnen (S)Wenn der Test anfängt zu funktionieren, wandert die Farbe über die Membran.
3. Warten Sie, bis die farbigen Bänder erscheinen. Das Ergebnis sollte innerhalb von 15 Minuten gelesen werden. Interpretieren Sie das Ergebnis nicht nach 20 Minuten.
[Interpretation der Ergebnisse]
POSITIV: Das Vorhandensein von zwei Linien als Kontrolllinie (C) und Prüflinie (T) im Ergebnisfenster zeigt ein positives Ergebnis an.
NEGATIV: Das Vorhandensein nur einer Steuerlinie (C) im Ergebnisfenster zeigt ein negatives Ergebnis an.Wenn die Steuereinheit (C) nach der Prüfung im Ergebnisfenster nicht sichtbar istEinige Ursachen für ungültige Ergebnisse sind, weil die Anweisungen nicht richtig befolgt wurden oder sich der Test nach Ablauf des Verfallsdatums verschlechtert hat.Es wird empfohlen, die Probe erneut mit einem neuen Test zu testen..
[QUALITÄTSKONTROLL]
• Innerliche Verfahrenskontrollen werden in die Prüfung einbezogen. Ein farbiges Band, das in der Kontrollregion (C) erscheint, gilt als interne positive Verfahrenskontrolle.Bestätigung eines ausreichenden Probenvolumens und einer korrekten Verfahrenstechnik.
• Externe Bedienelemente werden nicht mit diesem Kit geliefert.Es wird empfohlen, positive und negative Kontrollen als gute Laborpraxis zu testen, um das Prüfverfahren zu bestätigen und die ordnungsgemäße Testleistung zu überprüfen..
[Beschränkungen]
1Der cTnI-Schnelltest ist für die professionelle In-vitro-Diagnostik bestimmt und sollte nur zur qualitativen Erkennung von Herztroponin I verwendet werden.Aus der Farbintensität oder der Breite der sichtbaren Bands sollte keine Bedeutung abgeleitet werden..
2Der cTnI-Schnelltest wird nur auf das Vorhandensein von TroponinI in der Probe hinweisen und darf nicht als einziges Kriterium für die Diagnose eines Myokardinfarkts verwendet werden.
3Wenn das Testergebnis negativ ist und die klinischen Symptome bestehen bleiben, empfiehlt sich eine zusätzliche Untersuchung mit anderen klinischen Methoden.Der Test kann in Proben nicht weniger als 0,5 ng/mLofcTnI nachweisen.Ein negatives Ergebnis schließt das Vorhandensein von Troponin I im Blut nicht aus., da die Antikörper möglicherweise fehlen oder unter dem Mindestdetektionsgrad des Tests liegen.
4Wie bei allen diagnostischen Untersuchungen sollte eine bestätigte Diagnose erst von einem Arzt gestellt werden, nachdem alle klinischen und Laborbefunde ausgewertet wurden.
5Einige Proben, die ungewöhnlich hohe Titer heterophiler Antikörper mit rheumatoidem Faktor (RF) enthalten, können die erwarteten Ergebnisse beeinträchtigen.Eine weitere klinische Beurteilung sollte mit anderen dem Arzt zur Verfügung stehenden klinischen Informationen in Betracht gezogen werden..
[Leistungsmerkmal]
Relative Empfindlichkeit: 99,45%
Relative Spezifität: 99,52%
Gesamtabkommen: 99,49%

 Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!  Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!